Иванчикова главный внештатный клинический фармаколог Министерства здравоохранения Ярославской области |
|
История клинической фармакологии насчитывает немногим более полувека. В 1941 г. вышло в свет первое издание книги «Клиническая фармакология» Л.С. Гудмана и А. Гилмана. Как научная дисциплина клиническая фармакология возникла в середине XX века. Несколько выдающихся фармакологов, работавших в середине века, объединили фармакологию и «ноу-хау» в области применения лекарственных средств. Таким образом произошла трансформация оценки лекарств из состояния проб и ошибок в самостоятельную научную дисциплину. В СССР история клинической фармакологии связана с выдающимися учёными академиками Б.Е. Вотчалом, М.Д. Машковским, член-корреспондентом АМН СССР К.М. Лакиным, академиком РАН В.Г. Кукесом и др. 5 мая 1997 года министром здравоохранения Российской Федерации Т.Б. Дмитриевой был подписан Приказ №131 «О введении специальности „клиническая фармакология“». Эту дату можно считать днём рождения специальности «врач-клинический фармаколог» в России.Клиническая фармакология: что это такое
Структура*: Работа врача-клинического фармаколога включает: Работа главного внештатного клинического фармаколога: * соответствии с приказом Министерства здравоохранения РФ от 2 ноября 2012 г. N 575н “Об утверждении Порядка оказания медицинской помощи по профилю «клиническая фармакология», рекомендуемый штатный норматив составляет 1 ставку на 250 коек / 500 посещений в смену в медицинской организации Приказ Министерства здравоохранения РФ от 2 ноября 2012 г. N 575н “Об утверждении Порядка оказания медицинской помощи по профилю “клиническая фармакология”Служба клинической фармакологии Ярославской области
Нормативные документы, регулирующие лекарственное обеспечение
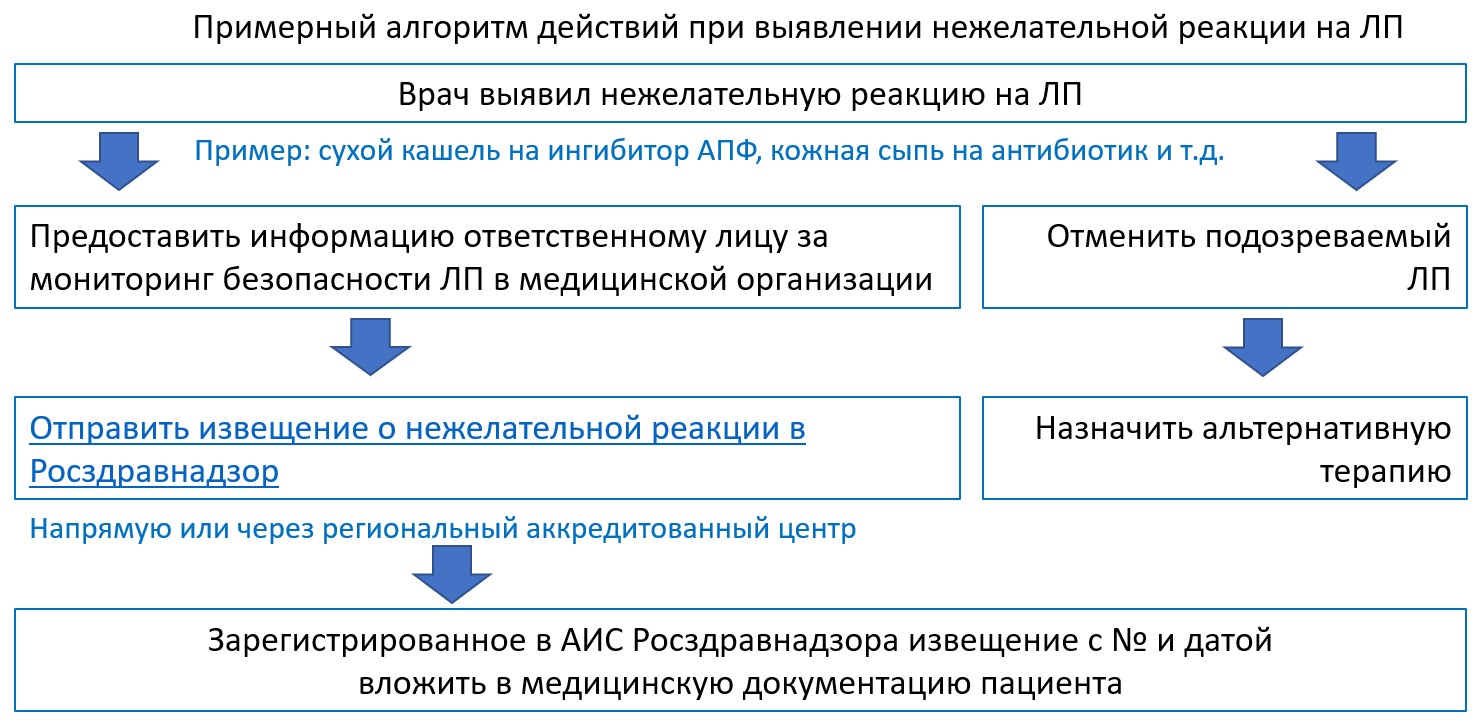
Медицинские организации обязаны сообщать в Росздравнадзор о нежелательных реакциях и иной информации по безопасности и эффективности, выявленной данной медицинской организацией, за исключением нежелательных реакций, выявленных в ходе проведения клинических исследований в срок, не превышающий 15 календарных дней* Медицинские организации обязаны в срок не более 3 рабочих дней сообщать в Росздравнадзор о серьезных нежелательных реакциях с летальным исходом или угрозой жизни, за исключением нежелательных реакций, выявленных в ходе проведения клинических исследований, проводимых в данной медицинской организации* Работа с нежелательными реакциями
NB! Новый приказ по фармаконадзору вступает в силу с 1 марта 2025 г. и действует до 1 марта 2031 г. Приказ Федеральной службы по надзору в сфере здравоохранения от 17 июня 2024 г. N 3518 Сайт Федеральной службы по надзору в сфере здравоохранения (Росздравнадзора)Действующие нормативные документы по фармаконадзору:
Полезные ресурсы